気体は、地表では大気中にありますが、地下では水に溶けています。地下において固体と気体との反応を考えるときに、水に気体がどのくらい溶けているかは重要です。ここでは、温度を上げると、気体が水へ溶ける量がどのように変化するかを見てみます。
水への気体の溶解度については、ヘンリーの法則があります。ヘンリーの法則とは、気体の分圧と水への溶解量とは比例するというものです。気体の分圧を上げるとそれに比例して水への溶解度も増えるのです。
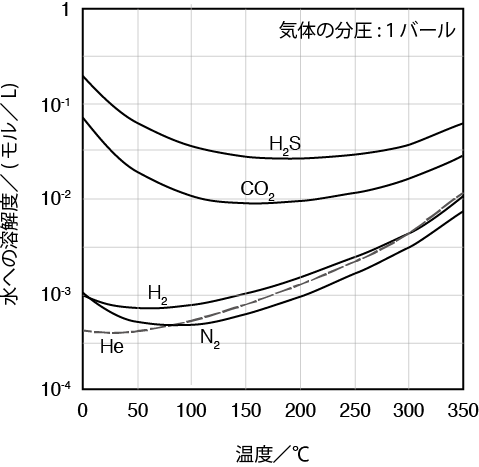
次に、水への気体の溶解度の温度依存性を見てみましょう。特に、100℃以上でどのようになるかを見ます。温度が上昇すると、水への気体の溶解度は減少すると中学や高校で習いました。確かに、図を見ると、硫化水素や二酸化炭素や窒素の水への溶解度は100℃までは温度上昇とともに減少しています。これは、温度が上昇すると分子の動きが活発になって大気中に気体分子が出て行くと説明されます。しかし、ヘリウムは25℃以上で温度上昇とともに溶解度が上昇しています。水素も50℃まで温度上昇とともに溶解度が減少していますが、80℃以上になると温度上昇とともに溶解度は増加に転じています。多くの場合、温度上昇で溶解度が上がることは例外であると説明されており、これ以上の説明がないことがほとんどです。
じつは、温度上昇とともに溶解度が増加するのは例外ではありません。100℃以上の溶解度のデータを見るとそれがわかります。高温領域では、温度上昇とともに、気体の溶解度はむしろ増加します。ヘリウム、水素、窒素では、100℃以上で、温度が上昇とともに溶解度が増加しています。これらの気体は、350℃で室温の10倍以上水に溶けます。二酸化炭素は160℃くらいで、硫化水素は190℃くらいで、温度が上昇とともに溶解度が増加し始めます。
高温で溶解度が高くなるのは、高温になると、水の性質が液体から気体に近い状態になるからです。水分子同士の結合が強い状態だと水と結合していない気体分子は邪魔なので、水は気体分子を追い出そうとします。しかし、温度が上がると、水は気体の状態に近づき水分子同士の結合が弱くなるので、水が気体分子を追い出そうとする力も弱くなり、多くの気体分子が水と共存できるのです。